Inventio
Vol. 21, núm. 54, 2025
doi: https://doi.org/10.30973/inventio/2025.21.54/9
Patrones dietéticos en enfermedad renal crónica: evidencias y recomendaciones nutricionales
Dietary patterns in chronic kidney disease: evidence and nutritional recommendations
Héctor Enrique Fabela Illescas
orcid: 0000-0003-4421-4409, fabelaillescashectorenrique@gmail.com
Universidad Vizcaya de las Américas, Campus Tulancingo de Bravo, Hidalgo (uva Tulancingo)
Fernanda Pamela González Vergara
orcid: 0009-0004-6569-3458, fernygonzalezvergara@gmail.com
Universidad Vizcaya de las Américas, Campus Tulancingo de Bravo, Hidalgo (uva Tulancingo)
Karla Yvette Gómez Becerra
orcid: 0000-0002-1447-5627, karlaivettegomezbecerra24@gmail.com
Doctorado en Ciencias de la Nutrición Traslacional, Centro Universitario de Ciencias de la Salud (cucs), Universidad de Guadalajara (udg)
Gabriel Betanzos Cabrera
orcid: 0000-0003-2027-6904, gbetanzo@uaeh.edu.mx
Instituto de Ciencias de la Salud (icsa), Universidad Autónoma del Estado de Hidalgo (uaeh)
resumen
La enfermedad renal crónica (erc) es un desafío global para la salud pública, no sólo por la carga significativa para los sistemas de salud, sino porque afecta la calidad de vida de millones de personas en todo el mundo. La relación entre la nutrición y la erc se ha convertido en un tema central de investigación debido a que la dieta cumple una función importante en la prevención y el tratamiento del paciente con erc. Algunos estudios han demostrado que los patrones dietéticos con énfasis en recomendaciones basadas en alimentos saludables son el estándar de oro para aumentar la esperanza de vida y reducir los riesgos de erc y la mortalidad. Aquí se describen algunos patrones dietéticos que pueden reducir la progresión de la erc.
palabras clave
enfermedad renal crónica, nutrición, patrón dietético, salud pública, calidad de vida
abstract
Chronic kidney disease (ckd) is currently a global public health challenge, not only because of the significant burden it places on healthcare systems but also because it affects the quality of life of millions of people worldwide. The relationship between nutrition and ckd has become a central topic of research, as diet plays a crucial role in the prevention and treatment of patients with ckd. Some studies have shown that dietary patterns emphasizing healthy foods are the gold standard for increasing life expectancy and reducing the risks of ckd mortality. Here are some dietary patterns that may slow the progression of ckd.
key words
chronic kidney disease, nutrition, dietary pattern, public health, quality of life
Recepción: 17/02/25. Aceptación: 16/06/25. Publicación: 12/11/25.
Generalidades e importancia del manejo nutricional
La enfermedad renal crónica (erc) es una enfermedad lenta y se caracteriza por la pérdida gradual de la función renal, que se manifiesta con una tasa de filtrado glomerular (tfg) menor a 60 mL/min/1.73m2 o una relación albúmina-creatinina urinaria >30mg/g (Yin et al., 2023). Esta condición afecta a una de cada diez personas en todo el mundo, lo que representa un importante problema de salud pública (Heindel et al., 2020). En México, durante 2021, se reportó que la prevalencia de erc fue de 9,184.9 casos por cada cien mil habitantes (Sevilla- González et al., 2025).
Las enfermedades crónicas no trasnmisibles (ecnt), como la diabetes, la obesidad, la hipertensión o la enfermedad cardiovascular, pueden conducir al desarrollo de la erc (Vallianou et al., 2019). No obstante, también puede presentarse de manera natural por el envejecimiento, la exposición a sustancias tóxicas o por infecciones (Snelson et al., 2017). Cuando se presenta la erc, la funcionalidad óptima de los riñones se ve comprometida, por lo que los pacientes y profesionales de la salud buscan formas de modificar el curso de la enfermedad para reducir su progresión.
La nutrición y los patrones dietéticos son factores modificables que se pueden utilizar para prevenir o retrasar la progresión de la erc (Snelson et al., 2017). La mayoría de las intervenciones dietéticas se centran en la reducción del consumo de macro y micronutrimentos, principalmente en aquellos con erc temprana. De acuerdo con algunos estudios, las dietas bajas en proteínas redujeron los riesgos de deterioro de la función renal y el empeoramiento de la albuminuria (Kasiske et al., 1998; Pedrini et al., 1996).
La erc se desarrolla a través de cinco etapas, las cuales pueden progresar a diferentes velocidades. Las primeras tres etapas de la enfermedad son consideradas como erc temprana. Las etapas 1 y 2 se caracterizan por la presencia de anomalías estructurales del riñón y por la existencia de proteinuria persistente o hematuria. Por su parte, la etapa 3 se define por una tfg entre treinta y 59 mL/min/1.73 m2 en al menos dos ocasiones, observadas en un intervalo mínimo de tres meses (Vallianou et al., 2019). En la etapa final de la erc, los riñones dejan de cumplir sus funciones vitales y el paciente requiere de otros tratamientos, como la diálisis o la hemodiálisis.
La progresión de la erc depende de muchos factores, como la inflamación de bajo grado, el estrés oxidativo, la proteinuria, la hipertensión y la diabetes; ésta última es la principal causa de erc. Sin embargo, se ha identificado que el principal contribuyente para la progresión de la erc es la mala calidad de la dieta (Bin Zarah et al., 2021).
La dieta contribuye de manera significativa al equilibrio ácido-base en la erc. Los nutrimentos pueden clasificarse como formadores de ácido o precursores de base. Los nutrimentos productores de ácido incluyen fósforo y aminoácidos que contienen azufre, como cisteína, metionina y taurina, mientras que los nutrimentos formadores de base incluyen potasio, magnesio y calcio.
En general, se considera que los alimentos de origen animal, como los productos cárnicos y los alimentos ultraprocesados, son precursores de ácido (figura 1); las frutas y verduras son productores de base, mientras que los productos lácteos y las leguminosas a menudo se consideran neutrales (Biruete et al., 2024).
La acidosis metabólica suele ser común en pacientes con erc y da como resultado un bajo nivel de bicarbonato plasmático, un factor de riesgo para la progresión de la nefropatía. Por lo tanto, en el manejo nutricional de la erc es esencial adoptar patrones alimentarios que favorezcan la función renal y reduzcan la acidosis metabólica. Un enfoque basado en proteínas de origen vegetal, como leguminosas, frutos secos y semillas, puede contribuir a una mejor homeostasis metabólica, mientras que la reducción de alimentos de origen animal y ultraprocesados minimiza la exposición a sodio, fosfatos añadidos y grasas trans, factores que pueden acelerar la progresión de la erc.
Además, un adecuado aporte de fibra a través de frutas y verduras frescas no sólo optimiza la microbiota intestinal, sino que también favorece la regulación de la acidosis metabólica, un riesgo común en la erc. Por ello es crucial equilibrar la ingesta de micronutrientes, priorizando fuentes naturales de potasio y magnesio, siempre según la función renal del paciente, para garantizar un enfoque nutricional que mejore el pronóstico y la calidad de vida.
Figura 1
Impacto en la erc por consumo por diferentes factores dietéticos
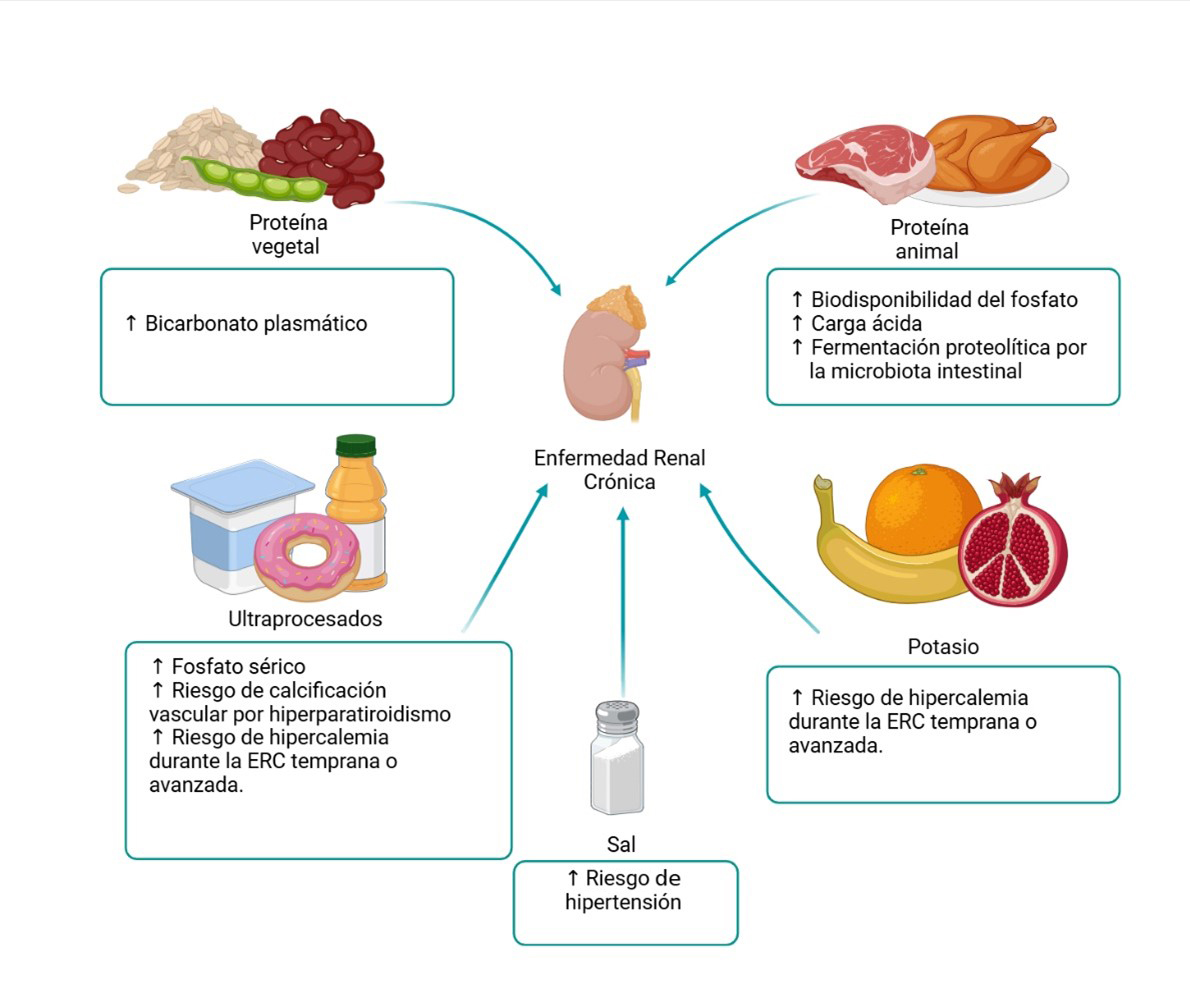
Fuente: elaboración propia.
Patrones dietéticos y sus efectos benéficos en la erc
Durante las últimas décadas, diversas investigaciones han respaldado el papel de las intervenciones nutricionales en el tratamiento de la erc. La terapia nutricional busca optimizar la calidad de la alimentación para mejorar el estado de salud de los pacientes (Naber y Purohit, 2021). En este sentido, los nefrólogos, nutriólogos y demás profesionales de la salud pueden considerar la adopción de patrones dietéticos enfocados en la calidad nutricional donde se dé prioridad a un mayor consumo de frutas y verduras. Este enfoque no sólo contribuye a un mejor aporte de fibra, vitaminas y minerales, sino que también puede ayudar a reducir el riesgo de desnutrición, una condición frecuente en pacientes con erc (Heindel et al., 2020).
Dieta dash
La dieta dash (dietary approaches to stop hypertension) es un patrón alimenticio para prevenir y controlar la hipertensión, considerada un factor de riesgo para la erc, la cual se ha demostrado que influye en el progreso de este padecimiento. Esta dieta se ha utilizado para tratar pacientes con erc, ya que, al preservar la función renal, pudiera tener un efecto benéfico. En un estudio de cohorte con seguimiento mayor a veinte años de quince mil participantes con riesgo de aterosclerosis en comunidades, se reportó que aquéllos con una mala adherencia a la dieta dash tenían un riesgo 16% mayor de erc incidente (Rebholz et al., 2016).
Durante las primeras etapas de la erc los patrones de alimentación basados en vegetales pueden reducir su progresión, ya que también se benefician de una reducción en la presión arterial (Snelson et al., 2017). Asimismo, otro estudio reportó que complementar la dieta con frutas y verduras para reducir la carga de ácidos no volátiles en un 50% —incluyendo aproximadamente de dos a cuatro tazas al día de la cantidad diaria habitual— no causó hipercalemia significativa en pacientes con erc en etapa 3 o 4 (Raphael, 2019).
En otro estudio de pacientes con erc etapa 4 éstos fueron seleccionados por tener un riesgo bajo de hipercalcemia. El tratamiento de la acidosis metabólica con vegetales productores de bases resultó eficaz para mejorar esta afección y reducir la función renal (Goraya et al., 2013). La intervención mediterránea-dash es la combinación de ambos patrones alimenticios que se ha asociado con menor incidencia de erc (Couch et al., 2024). Si bien se requiere mayor evidencia del uso de la dieta dash en pacientes con erc, es probable que los beneficios de las dietas basadas en plantas naturalmente altas en potasio y fibra y bajas en proteínas y minerales superen el riesgo potencial de desarrollar hipercalemia en la erc temprana (Snelson et al., 2017).
Dieta mediterránea
El patrón dietético mediterráneo tradicional se caracteriza por un consumo elevado de alimentos de origen vegetal —cereales, leguminosas, frutos secos, frutas y verduras y hierbas aromáticas—, una ingesta moderada-alta de pescado; una ingesta baja-moderada de productos lácteos; una ingesta baja en grasas saturadas, carne y aves de corral; una ingesta moderada de vino durante las comidas, y aceite de oliva, el cual es la principal fuente de grasa añadida.
Existe evidencia sólida que demuestra los efectos benéficos de la dieta mediterránea asociados a un menor riesgo cardiovascular y un menor riesgo de erc incidente (Yuzbashian et al., 2018), mediante una disminución de la inflamación sistémica, mejoría en el perfil lipídico y el metabolismo de las lipoproteínas. Además, favorece el control de la presión arterial, efectos benéficos sobre el control de la hiperglucemia, la hiperinsulinemia y la resistencia a la insulina. Este patrón también contribuye a reducir el estrés oxidativo y promueve cambios en la composición de la microbiota intestinal (Pérez-Torres et al., 2022).
Un ensayo predimed (prevention with mediterranean diet) demostró que una dieta mediterránea alta en grasas, suplementada con aceite de oliva virgen o frutos secos, la cual fue utilizada como prevención primaria para enfermedades cardiovasculares, resultó en una reducción de un 30% de eventos clínicos de enfermedad cardiovascular; además se encontró una protección significativa de la dieta mediterránea frente a la diabetes, lo que pudiera reducir la aparición de erc o su progresión (Martínez-Villaescusa et al., 2022).
Otro estudio demostró que el consumo de frutos secos y leguminosas se asoció con un riesgo reducido de progresión de erc. De igual forma, reportó que una ingesta alta de cereales y pescado, cuantificada mediante el sistema de puntuación de la dieta mediterránea, se asoció con una mayor tfg, lo que ha demostrado tener un efecto benéfico para los pacientes con erc. No obstante, una ingesta alta de lácteos bajos en grasa y enteros, un componente de la dieta mediterránea, se asoció significativamente con una tfg menor.
El consumo de productos lácteos bajos en grasa se recomienda en pacientes con erc, ya que se ha asociado con un menor riesgo de progresión de la enfermedad. Esto se debe, en parte, a su aporte de calcio, un mineral esencial en la regulación de la presión arterial y la salud ósea. Además, los productos lácteos bajos en grasa proporcionan proteínas de alto valor biológico sin una carga excesiva de grasas saturadas, cuya ingesta elevada se ha relacionado con efectos negativos en la función renal. Optar por lácteos descremados o semidescremados puede ser una estrategia nutricional beneficiosa dentro de un patrón dietético equilibrado (Heindel et al., 2020).
Dieta plado
La dieta plado (plant-dominant low-protein diet) es una dieta baja en proteínas y con predominio de alimentos de origen vegetal, la cual se centra en mejorar los síntomas ureicos, la seguridad, y se puede recomendar de manera segura a pacientes con erc temprana o avanzada. Para implementar esta dieta se recomienda seguir una fase inicial de adaptación durante los primeros tres meses. Posteriormente, se establece un patrón alimentario bajo en proteínas, con un aporte de 0.6-0.8 g/kg/día, asegurándose de que al menos el 50% de ellas provengan de fuentes vegetales, como garbanzo, chía y amaranto. Además, se recomienda alcanzar un consumo mínimo de 25 g de fibra al día, lo que contribuye a la salud intestinal y metabólica del paciente con erc. Los pacientes deben estar en constante monitoreo, aproximadamente cada tres o seis meses, donde se realice una evaluación dietética de acuerdo con sus necesidades (Kalantar-Zadeh et al., 2020).
Una ingesta de proteína animal elevada interfiere con la capacidad del riñón para autorregular el flujo sanguíneo capilar glomerular, al activar mediadores humorales y locales que vasodilatan la arteriola aferente. Después de la ingesta de carne, tanto el flujo sanguíneo renal como la tfg aumentan. De hecho, cuando las personas con función renal normal pasan de una ingesta baja de proteína animal a una alta, tanto el flujo sanguíneo renal como la tfg pueden aumentar hasta un 30%. Este aumento del flujo sanguíneo renal se limita a la ingesta de proteína animal, y las personas que siguen una dieta vegetariana suelen tener una tfg más baja en comparación con las personas que consumen proteína animal. Esta dilatación arteriolar aferente se produce debido a que los aminoácidos de las proteínas activan múltiples mediadores humorales y locales que vasodilatan la arteriola aferente (Kramer, 2019).
Algunas ventajas de este patrón alimenticio es que no interfiere con los medicamentos; por el contrario, suele tener efecto sinérgico o potenciador (Kalantar-Zadeh et al., 2020). A pesar de la importancia de la nutrición en el manejo de la erc, muchos pacientes no reciben asesoría especializada antes de iniciar la diálisis. Esta situación no sólo refleja la falta de información por parte de los pacientes, sino también la necesidad de que los profesionales de la salud se capaciten en estrategias nutricionales adaptadas a la erc. La ausencia de un tratamiento nutricional personalizado y el desconocimiento sobre los distintos patrones dietéticos pueden comprometer el pronóstico del paciente con erc, lo cual afecta su calidad de vida y su evolución clínica.
Dieta de la milpa
Este patrón dietético se caracteriza por una dieta rica en aquellas verduras y frutas que comúnmente son cultivadas en la región mesoaméricana (México central y Centroamérica), así como cereales integrales y pescado. Asimismo, se recomienda evitar alimentos ultraprocesados, carnes rojas y edulcorantes artificiales y se promueve un estilo de vida saludable, la práctica de actividad física, el consumo de agua y el bienestar general. Si bien este patrón alimentario tiene características similares a las de las dietas mediterránea y dash, puede ser más concordante culturalmente con las personas de la región de Mesoamérica (Biruete et al., 2024).
En este patrón se enfatizan los alimentos productores de base y los alimentos neutrales, característica que puede tener un impacto positivo en los pacientes con acidosis metabólica¡ o que se encuentren en riesgo de padecerla, en particular aquellos con erc etapa 3 y superior. Además, este patrón alimenticio se caracteriza por ofrecer múltiples beneficios, como el equilibrio ácido-base. Al incluir fuentes de proteína vegetal, se aporta calcio, magnesio y fibra soluble e insoluble, lo que favorece la absorción de colesterol y la gestión de potasio y fósforo.
De manera adicional, este patrón contribuye a la modulación de la microbiota intestinal, la reducción de la inflamación y la adecuación cultural (Crocker Sagastume y Navarro Ponce, 2023). También promueve el balance de grasas saturadas e insaturadas, y dentro de éstas, lo que reduce la inflamación sistémica producida por las ecnt, principalmente la diabetes, la hipertensión y el sobrepeso, lo cual previene problemas renales y de desmineralización. Sin embargo, se necesitan ensayos que prueben su eficacia en la erc (Biruete et al., 2024).
Dietas cetogénicas muy bajas en calorías
Las dietas cetogénicas muy bajas en calorías son intervenciones dietéticas que imitan el ayuno, y se caracterizan por una ingesta baja de calorías e hidratos de carbono (<20 g/día), 1-1.5 g de proteína/kg de peso corporal ideal, 15-30 g de grasa/día y una ingesta calórica de alrededor de 500-800 kcal/día. Usualmente se utilizan en pacientes con obesidad, pero, debido al aumento de la ingesta de proteínas, se consideran dañinas para la función renal y no se recomiendan en sujetos con filtración reducida. Sin embargo, en un estudio observacional prospectivo realizado con 92 pacientes que siguieron la dieta, la cual estaba constituida por una ingesta calórica entre 450 y 800 kcal/día y un consumo de hidratos de carbono entre 20 g y 50 g/día, durante aproximadamente tres meses, 38 tenían erc temprana y 54 no tenían ninguna afección renal, por lo que fueron tomados como grupo control.
Se colectaron datos antropométricos, impedancia bioeléctrica y datos bioquímicos antes y al final de la intervención dietética. Tras la estratificación de la función renal, no se encontraron diferencias en los resultados de eficacia y seguridad. No obstante, un 27.7% de los pacientes con erc temprana informó de una normalización del filtrado glomerular tras la intervención dietética, por lo que los autores del estudio concluyeron que, cuando la dieta se realiza bajo la supervisión de profesionales de la salud o especialistas, podría ser un tratamiento eficaz y seguro para la pérdida de peso en pacientes con obesidad, incluidos aquellos que presentan erc temprana (Bruci et al., 2020).
Los efectos benéficos más destacados de este patrón alimenticio incluyen la disminución de la hiperinsulinemia y el control de la diabetes, lo que se traduce en valores reducidos de albúmina glucosilada y glucosa capilar. Por esta razón, este patrón alimenticio podría emplearse en pacientes con erc, siempre y cuando se encuentren bajo la supervisión de un profesional de la salud (Stasi et al., 2022). Sin una adecuada vigilancia, existe el riesgo de desequilibrios en la ingesta de proteínas, micronutrientes y energía, lo que podría afectar la estabilidad metabólica y la calidad de vida del paciente. Por ello, su implementación debe ser personalizada y monitoreada regularmente para garantizar su seguridad y eficacia.
Conclusión
La dieta cumple una función clave en la progresión de la erc. Patrones como las dietas mediterránea, dash, plado y la de la milpa parecen ser opciones seguras y saludables para reducir la aparición o progresión de erc, mientras que la dieta cetogénica baja en calorías requiere más evidencia para ser una alternativa en pacientes con erc. Aunque los enfoques dietéticos muestran beneficios, se necesita mayor investigación para conocer su repercusión en esta enfermedad.
Referencias
Bin Zarah, A., Feraudo, M. C. y Andrade, J. M. (2021). Development and relative validity of the chronic kidney disease short food frequency questionnaire (ckd sffq) to determine diet quality and dietary habits among adults with chronic kidney disease. Nutrients, 13(10), 3610. https://doi.org/10.3390/nu13103610
Biruete, A., Leal-Escobar, G., Espinosa-Cuevas, Á., Mojica, L. y Kistler, B. M. (2024). Dieta de la milpa: a culturally-concordant plant-based dietary pattern for hispanic/latine people with chronic kidney disease. Nutrients, 16(5), 574. https://doi.org/10.3390/nu16050574
Bruci, A., Tuccinardi, D., Tozzi, R., Balena, A., Santucci, S., Frontani, R., Mariani, S., Basciani, S., Spera, G., Gnessi, L., Lubrano, C. y Watanabe, M. (2020). Very low-calorie ketogenic diet: a safe and effective tool for weight loss in patients with obesity and mild kidney failure. Nutrients, 12(2), 333. https://doi.org/10.3390/nu12020333
Couch, C. A., Ament, Z., Patki, A., Kijpaisalratana, N., Bhave, V., Jones, A. C., Armstrong, N. D., Cheung, K. L., Kimberly, W. T., Tiwari, H. K. e Irvin, M. R. (2024). The mediterraneandash Intervention for Neurodegenerative Delay (mind) Diet and Metabolites in Chronic Kidney Disease. Nutrients, 16(15), 2458. https://doi.org/10.3390/nu16152458
Crocker Sagastume, R. C. y Navarro Ponce, G. Á. (2023). Educación disruptiva intercultural en la promoción de dieta de la milpa en enfermedades crónicas. Revista Latinoamericana de Estudios Educativos, 53(3), 335-358. https://doi.org/10.48102/rlee.2023.53.3.580
Goraya, N., Simoni, J., Jo, C. H. y Wesson, D. E. (2013). A comparison of treating metabolic acidosis in ckd stage 4 hypertensive kidney disease with fruits and vegetables or sodium bicarbonate. Clinical Journal of the American Society of Nephrology, 8(3), 371-381. https://doi.org/10.2215/CJN.02430312
Heindel, J., Baid-Agrawal, S., Rebholz, C. M., Nadal, J., Schmid, M., Schaeffner, E., Schneider, M., Meiselbach, H., Kaesler, N. Bergmann, M. Ernst, S., Krane, V., Eckardt, K.-U., Floege, J., Schlieper, G., Saritas, T. y gckd Study Investigators (2020). Association between dietary patterns and kidney function in patients with chronic kidney disease: a cross-sectional analysis of the german chronic kidney disease study. Journal of Renal Nutrition, 30(4), 296-304. https://doi.org/10.1053/j.jrn.2019.09.008
Kalantar-Zadeh, K., Joshi, S., Schlueter, R., Cooke, J., Brown-Tortorici, A., Donnelly., M., Schulman, S., Lau, W.-L., Rhee, C. M., Streja, E., Tantisattamo, E., Ferrey, A. J., Hanna, R., Chen, J. L. T., Malik, S., Nguyen, D. V., Crowley, S. T. y Kovesdy, C. P. (2020). Plant-dominant lowprotein diet for conservative management of chronic kidney disease. Nutrients, 12(7), 1931. https://doi.org/10.3390/nu12071931
Kasiske, B. L., Lakatua, J. D., Ma, J. Z. y Louis, T. A. (1998). A meta-analysis of the effects of dietary protein restriction on the rate of decline in renal function. American Journal of Kidney Diseases, 31(6), 954-961. https://doi.org/10.1053/ajkd.1998.v31.pm9631839
Kramer, H. (2019). Diet and chronic kidney disease. Advances in Nutrition, 10, supl. 4, S367-S379. https://doi.org/10.1093/advances/nmz011
Martínez-Villaescusa, M., Aguado-García, Á., López-Montes, A., Martínez-Díaz, M., Gonzalvo-Díaz, C., Pérez-Rodriguez, A., Pedrón-Megías, A., García-Arce, L., Sánchez-Sáez, P., García-Martínez, C., Azaña-Rodríguez, A., García-Martínez, A. B., Andrés-Pretel, F., Botella-Romero, F., Vega-Martínez, A., Giménez Bachs, J. M. y León-Sanz, M. (2022). New approaches in the nutritional treatment of advanced chronic kidney disease. Nefrología (English Edition), 42(4), 448-459. https://doi.org/10.1016/j.nefroe.2022.11.001
Naber, T. y Purohit, S. (2021). Chronic kidney disease: role of diet for a reduction in the severity of the disease. Nutrients, 13(9), 3277. https://doi.org/10.3390/nu13093277
Pedrini, M. T., Levey, A. S., Lau, J., Chalmers, T. C. y Wang, P. H. (1996). The effect of dietary protein restriction on the progression of diabetic and nondiabetic renal diseases: a meta-analysis. Annals of Internal Medicine, 124(7), 627-632. https://doi.org/10.7326/0003-4819-124-7-199604010-00002
Pérez-Torres, A., Caverni-Muñoz, A. y González García, E. (2022). Mediterranean diet and chronic kidney disease (ckd): a practical approach. Nutrients, 15(1), 97. https://doi.org/10.3390/nu15010097
Raphael, K. L. (2019). The Dietary Approaches to Stop Hypertension (dash) diet in chronic kidney disease: should we embrace it? Kidney International, 95(6), 1296-1298. https://doi.org/10.1016/j.kint.2019.01.026
Rebholz, C. M., Crews, D. C., Grams, M. E., Steffen, L. M., Levey, A. S., Miller iii, E. R., Appel, L. J. y Coresh, J. (2016). dash (Dietary Approaches to Stop Hypertension) diet and risk of subsequent kidney disease. American Journal of Kidney Diseases, 68(6), 853-861. https://doi.org/10.1053/j.ajkd.2016.05.019
Sevilla-González, M., González-Ortiz, A., Landa-Anell, M. V., Melgarejo-Hernández, M. A., Arias-Marroquín, A. T., Del Razo-Olvera, F. M., Román-Calleja, B. M., Monreal-Lugo, A. V., Martin-Vences, A. J., Haua-Navarro, K. y Espinosa-Cuevas, A. (2025). Adaptation of the nutrition care process in metabolic diseases in the mexican population. Frontiers in Nutrition, 12, 1513747. https://doi.org/10.3389/fnut.2025.1513747
Snelson, M., Clarke, R. E. y Coughlan, M. T. (2017). Stirring the pot: can dietary modification alleviate the burden of ckd? Nutrients, 9(3), 265. https://doi.org/10.3390/nu9030265
Stasi, A., Cosola, C., Caggiano, G., Cimmarusti, M. T., Palieri, R., Acquaviva, P. M., Rana, G. y Gesualdo, L. (2022). Obesity-related chronic kidney disease: principal mechanisms and new approaches in nutritional management. Frontiers in Nutrition, 9, 925619. https://doi.org/10.3389/fnut.2022.925619
Vallianou, N. G., Mitesh, S., Gkogkou, A. y Geladari, E. (2019). Chronic kidney disease and cardiovascular disease: is there any relationship? Current Cardiology Reviews, 15(1), 55-63. https://doi.org/10.2174/1573403X14666180711124825
Yin, L., Dong, X., Liao, W., Liu, X., Zheng, Z., Liu, D., Wang C. y Liu, Z. (2023). Relationships of beans intake with chronic kidney disease in rural adults: a large-scale cross-sectional study. Frontiers in Nutrition, 10, 1117517. https://doi.org/10.3389/fnut.2023.1117517
Yuzbashian, E., Asghari, G., Mirmiran, P., Amouzegar-Bahambari, P. y Azizi, F. (2018). Adherence to low-sodium Dietary Approaches to Stop Hypertension-style diet may decrease the risk of incident chronic kidney disease among high-risk patients: a secondary prevention in prospective cohort study. Nephrology Dialysis Transplantation, 33(7), 1159-1168. https://doi.org/10.1093/ndt/gfx352